ГКС и НПВС при артрите
Глюкокортикостероиды (ГКС) используются в лечении многих ревматических заболеваний в качестве базисной противовоспалительной терапии (Чичасова Н.В., 2014) (Нуруллина Г.И., 2013). Из всех известных противовоспалительных ЛС только ГКС действуют на подавляющее большинство известных провоспалительных цитокинов и подавляют функции иммунных клеток практически всех типов, то есть ГКС фактически характеризуются универсальностью как противовоспалительного, так и иммунотропного действия (Рекалов Д.Г., 2013) (Hochberg M.C., Rheumatology, 2011) (Firestein G.S., 2008).
Между тем, место ГК в лечении пациентов с РА широко обсуждается ревматологическим сообществом уже более 60 лет (Чичасова Н.В., 2014), что обусловлено, в первую очередь, экстраординарным сочетанием высокой терапевтической активности с широким спектром неблагоприятных, а порой и серьезных, нежелательных эффектов, которые, в конечном итоге, в случае применения ГКС в высоких терапевтических дозах полностью нивелируют благоприятный исход терапии пациентов с РА.
Для решения вопроса о поиске оптимального баланса между эффективностью и безопасностью ГКС разрабатывались различные терапевтические режимы их применения, в частности альтернативный режим, внутривенное введение, депо-инъекции (интрасуставные), причем эти режимы стали применять при отсутствии данных рандомизированных контролируемых исследований, то есть научных доказательств (Чичасова Н.В., 2014). При этом почти 30 лет спустя применения таких альтернативных режимов в ревматологической практике в рамках одного мета-анализа базы данных Arthritis, Rheumatism, and Aging Medical Information System (ARAMIS) было установлено, что у пациентов с РА, получавших ГКС, риск преждевременной летальности был в 1,5 раза выше, чем у пациентов, не получавших ГКС-терапии (Wolfe F M. D., 1994)
Быстрый эффект и подчас тяжелые отдаленные последствия, необходимость медленного снижения дозы и сохраняющаяся возможность обострения, нередко негативное отношение больных к ГК и, напротив, чрезмерное «увлечение» некоторых клиницистов этим видом терапии послужили предпосылкой к более вдумчивому и осторожному подходу применения ГКС у пациентов с РА и стремления уменьшить их кумулятивную дозу (Чичасова Н.В., 2014).
Для ревматологов стало аксиомой, что назначение ГКС в относительно низких дозах оправдано в ранних стадиях РА, а высокие дозы используются только по строгим показаниям:
- очень высокая активность ревматоидного процесса, в том числе с явлениями генерализованного васкулита (лихорадка, снижение массы тела, анорексия и др.);
- тяжелые осложнения терапии DMARD.
В остальных случаях назначение при РА ГКС в высоких дозах и в течение длительного времени абсолютно противопоказано и может рассматриваться как серьезная врачебная ошибка.
Согласно последним рекомендациям EULAR 2013 г. (Smolen JS, 2014):
- в качестве компонента стратегии лечения в течение первых 6 мес РА следует рассматривать применение низких доз ГКС56 (в комбинации с одним или несколькими DMARD;
- особо подчеркивается, что ГКС следует отменить так быстро, насколько это возможно с клинической точки зрения57;
- монотерапия ГКС не рекомендуется и может назначаться только в виде исключения, когда применение всех других DMARD и биологических препаратов противопоказано; при лечении ГКС должна проводиться профилактика осложнений (в частности немедленное назначение противоостеопоротической терапии).
Результаты недавних исследований продемонстрировали, что по рентгенологическим признакам и данным магнитно-резонансной томографии (МРТ), ГКС показали эффективность относительно снижения скорости прогрессирования костно-хрящевой деструкции в пораженных суставах. ГКС в малых дозах (<7,5 мг преднизолона в день) используются в лечении около 1/3 пациентов с РА. Значительное количество больных РА начинают прием ГКС в качестве инициальной терапии. Несмотря на это, терапия ГКС ассоциируется с т высокую частоту развития таких побочных эффектов, как истончение кожи, катаракта, гастропатии, остеопороз, артериальная гипертензия и гиперлипидемия, что предполагает развитие указанных нежелательных побочных явлений при назначении ГКС. Таким образом, всем пациентам, которые принимают ГКС, целесообразно назначение препаратов кальция (от 1200 МЕ в сутки) с витамином D (800 МЕ в сутки), ИПП, антирезорбтивных средств, антигипертензивных препаратов т.д. (Чичасова Н.В., 2014)
Нестероидные противовоспалительные средства (НПВС). До 1990-х гг. существовала стратегия «терапевтической пирамиды», предусматривающая использование в течение нескольких месяцев НПВС, а только затем – DMARD(Mikuls T.R., O’Dell J., 2000). В настоящее же время, как упоминалось выше, терапевтические стратегии направлены помимо купирования болевого синдрома на предупреждение деструктивных процессов, минимизацию скованности в суставах и, как следствие, сохранение способности выполнения пациентами с РА повседневных функций (сохранение функционального статуса) и улучшение/сохранение качества жизни.
Пациенты с РА нуждаются практически в непрерывной терапии НПВС (Балабанова Р.М., Федина Т.П., 2004), что обусловлено хроническим характером болевого синдрома при ревматических заболеваниях, вызванного развитием воспаления в синовиальной оболочкесуставов в связи с гиперпродукцией провоспалительных цитокинов, модуляцией функций иммунокомпетентных клеток и их пролиферацией, деструктивным действием протеаз. При этом согласно рекомендациям ВОЗ, первой ступенью лечения хронической боли при ревматических заболеваниях являются неопиоидные анальгетики из группы НПВС, оказывающие хороший анальгетический эффект при слабой и умеренной боли (Раскина Т.А., 2011).
Однако применение НПВС обеспечивают лишь частичное уменьшение артралгического (суставного) синдрома и продолжительности периода утренней скованности. Так, в ходе многочисленных исследований при применении НПВС не удалось продемонстрировать структурные РА-модифицирующие эффекты, в связи с чем, очевидно, их целесообразно назначать только в комбинациях с DMARD и глюкокортикостероидами. В то же время, даже в случаях кратковременного приема и в небольших дозах НПВС могут становиться причиной развития НПВС-гастродуаденопатий, риск которых увеличивается с возрастом и при наличии в анамнезе язвенной болезни желудка или двенадцатиперстной кишки (Рекалов Д.Г., 2013)(Балабанова Р.М., Федина Т.П., 2004)(Раскина Т.А., 2011).
Следует также отметить, что проблема терапии РА нередко осложняется экстрасуставными проявлениями заболевания, в том числе со стороны ЖКТ. Так, в гастроэнтерологические проявления РА могут ассоциироваться с рефлюкс-эзофагитом, инфарктами и язвами стенки кишечника, энтеропатией кровотечениями из вен пищевода и рядом другим (Абдулганиева Д.И., Салихов И.Г., 2011). Таким образом, гипотетически эффекты НПВС на ЖКТ могут интерферировать с гастроинтестинальными проявлениями РА и в значительной степени ухудшать прогноз заболевания и исходы терапии.
Так, в частности в одном отечественном исследовании осложнения язвенной болезни на фоне приема НПВС наиболее часто отмечались в группе пациентов с РА, в частности получавших диклофенак. В группе больных с АС и ОА осложнений язвенной болезни не зарегистрировано. Наличие в последние 3 мес неприятных ощущений со стороны ЖКТ отмечало абсолютное большинство больных (Рисунок). При этом больные РА, получавшие ацеклофенак, указывали на такие ощущения в 100% случаев. В целом из Рисунка 13 видно, что жалобы на неприятные ощущения в ЖКТ на фоне приема различных препаратов НПВС в группе пациентов с РА отмечались значительно чаще в сравнении с пациентами с анкилозирующимспондилоартритом или остеоартритом (Раскина Т.А., 2011).
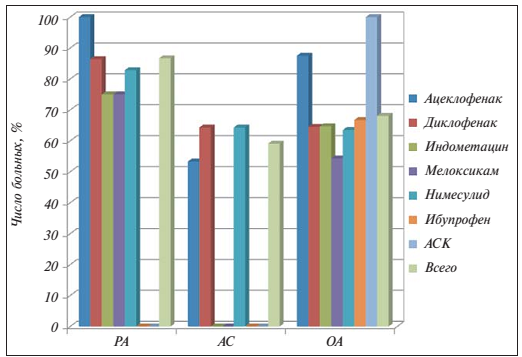
Рисунок 14. Наличие неприятных ощущений со стороны ЖКТ на фоне 3-месячного приема НПВС пациентами с ревматоидным артритом (РА), анкилозирующим спондилитом (АС) или остеоартритом (ОС) (Раскина Т.А., 2011)
Нежелательные эффекты НПВС не ограничиваются их гастроинтестинальной токсичностью. НПВС могут также потенцировать риск задержки натрия, повышения АД, сердечно-сосудистой недостаточности, гематологической токсичности и ряда других НПВС-индуцированных осложнений.
Специфические ингибиторы ЦОГ-2 отличаются лучшим профилем безопасности, в первую очередь, в отношении язвенных поражений ЖКТ и поражений системы кроветворения, не подавляют активность фермента ЦОГ-1, обладающего протективными свойствами в отношении слизистых ЖКТ. В сравнительных исследованиях продемонстрировано, что при использовании селективных ингибиторов ЦОГ-2 частота развития гастропатий приблизительно на 50% меньше по сравнению с традиционными НПВС (FitzGerald G.A., Patrono С., 2001) (SilversteinF.E., 2000).
Добавление ингибиторов протонной помпы (в т.ч. омепразол) в схемы лечения с НПВС также уменьшает процент кровотечений, связанных с применением обычных НПВС (ChanF.K.L., 2002). Эффективность ингибиторов ЦОГ-2 превосходит эффективность более ранних и менее дорогих НПВС (KirwanJ.R., 1995). Особо стоит отметить, что ингибиторы протонной помпы (омепразол) могут вызывать и/или усугублять процессы уменьшения минеральной плотности костной ткани, что у пациентов с РА, имеющих различные дисгормональные нарушения, часто в постменопаузальном периоде, чревато развитием различных низкоэнергетических переломов. Традиционные НПВС («золотой стандарт» – диклофенак натрия) и ингибиторы ЦОГ-2 обладают также нефротоксическим действием и способны вызывать тромботические события не только у предрасположенных к этим состояниям пациентов, но и у здоровых лиц (FitzGerald G.A., Patrono С., 2001).
Определенной эффективностью и отсутствием общей токсичности обладают НПВС, применяемые локально в виде мазей, кремов и гелей. Местное нанесение препаратов практически не имеет противопоказаний и допустимо в любом возрасте, независимо отналичия сопутствующих заболеваний, и может рассматриваться в качестве дополнения к системному назначению НПВС. В ряде случаев локальные НПВС позволяют снизить дозу пероральной формы последних. Благоприятные результаты дает 3-4 -кратное нанесение локального средства в течение суток в оптимальной терапевтической «дозе» с учетом выраженности воспалительного процесса, величины пораженного сустава и состояния кожного покрова (Балабанова Р.М., Федина Т.П., 2004). В то же время, очевидно, что эффективность НПВС для локального применения на фоне РА существенно лимитирована отсутствием клинически значимых эффектов на аутоиммунологические звенья патогенеза и системные проявления заболевания.
‹‹ Предыдущая Следующая ››
Автор материала: Булгакова Яна Сергеевна, кандидат биологических наук, ООО Сайнсфайлз
Понравилась статья? Поделись с друзьями!
Также стоит почитать:
Загрузка...



























 Важно знать:
Важно знать: Полезно:
Полезно: Интересно:
Интересно:




